Chap 15. Л§УМАшРЧ ППЊЧа
Chap 16. ATPПЭ АэПЁГЪСі ШЧеЙА
metabolism (ЙАСњглоѓ)
Л§УМ ГЛПЁМ РЯОюГЊДТ ЙАСњКЏШПЁ ДыЧб БЄРЧРЧ ПыОюЗЮМ
СМРК РЧЙЬЗЮДТ ПЁГЪСіДыЛч, СіЙцДыЛч, ЕюРИЗЮ БИКаЕШДй.
ЙАСњДыЛч: ЕЖИГПЕОчЛ§ЙААњ СОМгПЕОчЛ§ЙАПЁ РЧЧб МјШЏРЬ РЬЗчОюСјДй.
catabolic: КаЧиАњСЄРИЗЮ ХКШМіМв ШЧеЙАРЧ ЛъШАњСЄРЬ МіЙнЕЧИч ПЁГЪСіАЁ Л§МКЕШДй.
anabolic : Л§ЧеМК АњСЄРИЗЮ ШЏПјАњСЄРЬ МіЙнЕЧИч ПЁГЪСіАЁ МвИ№ЕШДй.
1. ПЁГЪСі
И№Еч Л§ЙАЧаРћ ЙнРРПЁДТ ПЁГЪСі РќШЏРЬ ЦїЧдЕШДй. ЛъШАњСЄПЁМ ЙцУтЕШ ПЁГЪСіПЭ ШЏПјАњСЄПЁ РЬПыЕЧДТ ПЁГЪСіДТ ЕПРЯЧб ЧќХТРЧ АЭРИЗЮМ РњРх, РЬПыЕШДй.
ЙАСњРЧ ДыЛчПЁМ ЙцУтЕЧДТ ПЁГЪСіДТ Л§ЙАУМПЁМ БтАшРћ, П, Кћ, РќБт, ШЧаРћ ПЁГЪСі ЕюРИЗЮ РќШЏЕШДй. ПЁГЪСіРЧ ШхИЇРК РЯЙцЧтРЬДй. ПАњ ПЃЦЎЗЮЧЧЗЮ ЙцУтЕЧДТ ПЁГЪСіДТ Л§ЙАУМПЁ РЧЧи РЬПыЕЩ Мі ОјДй.
1-1. ШЧаЙнРРРЧ ППЊЧа
(1) Аш: ЙнРРАшПЭ ПмАшИІ ЦїЧдЧЯДТ ПьСжАш
(Universe= reacting system + surrounding)
ЙнРРАшДТ ДнШљАш, АэИГАш, АГЙцАшЗЮ БИКаЕШДй. ДнШљАш (closed system)ПЁМДТ ЙАСњАњ ПЁГЪСіРЧ БГШЏРЬ ОјРИИч, АэИГАш (isolated system)ПЁМДТ ПЁГЪСіРЧ БГШЏИИРЬ РЯОюГДй. Л§ЙАРК АГЙцАш (open system)ПЁ ЧиДчЕЧИч ПЁГЪСіПЭ ЙАСњРЧ БГШЏРЬ РЯОюГДй.
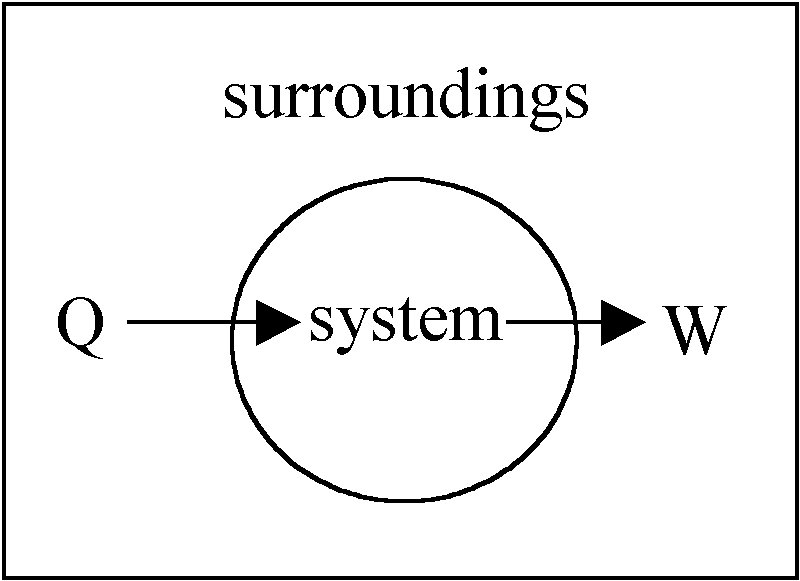
(2) ППЊЧа СІ1Й§ФЂ: ПЁГЪСі КИСИРЧ Й§ФЂ

ПьСж ГЛРЧ Уб ГЛКЮПЁГЪСіДТ РЯСЄЧЯДй. ОюЖВ ЙАИЎШЧаРћ КЏШПЁМЕчСі ПЁГЪСіРЧ ЧќХТДТ ЙйВюСіИИ РќУМ ПЁГЪСіДТ РЯСЄЧЯАд РЏСіЕШДй. ЙЎСІДТ ПЁГЪСіДТ МјШЏЕЧСі ОЪБт ЖЇЙЎПЁ ОѓИЖГЊ ГєРК ШПРВЗЮ ОђРЛ Мі РжРИГФ ЧЯДТ АЭРЬДй.
МіНФРИЗЮ ЧЅЧіЧЯИщ, ГЛКЮПЁГЪСіРЧ КЏШ ЁтE = EB-EA = q + w РЬДй (БзИВ ТќСЖ).
БтАшРћРЮ РЯПЁИИ БЙЧбЧбДйИщ ЁтE = qЗЮМ РЯСЄКЮЧЧАњСЄПЁМДТ РЏПыЧЯДй. БзЗЏГЊ ШЧа,Л§ШЧаРћ ЙнРРРК РЯСЄОаЗТПЁМ ЧрЧиСіДТ АцПьАЁ ИЙРИЙЧЗЮ РЬПЁ РћЧеЧб ЛѕЗЮПю ЧдМі HИІ СЄРЧЧЯАд ЕШДй. КЮЧЧРЧ КЏШАЁ АХРЧ ОјРЛ АцПь ЁтH Ёж ЁтE ЖѓДТ НФРЬ ОђОюСјДй. Ся, РЯСЄОаЗТАњСЄПЁМ ЁтHДТ РЬЕПЕЧДТ ПАњ ААОЦСјДй. ЕћЖѓМ ГЛКЮПЁГЪСіРЧ КЏШ (ЁтE)ДТ ЙнРРПРЧ КЏШ (ЁтH) ЗЮМ НБАд УјСЄЕЩ Мі РжДй. H (enthalpy)ДТ ЙнРРАшРЧ ПЗЎ (ЙнРРП)ЗЮМ ЙнРРЙААњ Л§МКЙАРЧ ШЧаАсЧеРЧ МіПЭ СОЗљИІ ЙнПЕЧбДй.
ШэПЙнРРПЁМ ЁтH ЁЕ0 РЬДй. Л§МКЙАРК ЙнРРЙАКИДй ГЗРК ПЗЎРЛ АЁСјДй.
ЙпПЙнРРПЁМ ЁтHЁД 0 РЬДй. Л§МКЙАРК ЙнРРЙАКИДй ГєРК ПЗЎРЛ АЁСјДй.
РкЙпРћРИЗЮ СјЧрЕЧДТ ДыКЮКаРЧ ЙнРРРК ЙпПЙнРРРИЗЮ ЁтHРЧ АЈМвАЁ РЯОюГДй. БзЗИСіИИ (NH4)2SO4АЁ ЙАПЁ ГьДТ АцПьПЭ ААРК ШэПЙнРРРЧ АцПьЕЕ ЙнРРРЬ СјЧрЕШДй. РЬДТ ПЃЦЎЗЮЧЧРЧ СѕАЁПЁ РЧЧб АЭРИЗЮ (СѕАЁЧЯДТ ПАРЧ ПЃЦЎЗЮЧЧПЭ АЈМвЧЯДТ ЙА КаРкРЧ ПЃЦЎЗЮЧЧРЧ ТїПЁ РЧЧб ШПАњ), ЕћЖѓМ ЙнРРПЗЮДТ ЙнРРРЧ РкЙпМКРЛ ГэРЧЧв Мі ОјДйДТ АЭРЛ АЁИЎХВДй.
(2) ППЊЧа СІ 2 Й§ФЂ: ЙЋСњМРЧ Й§ФЂ
АшДТ СЄЕЗЕШ ЛѓХТЗЮКЮХЭ ЙЋСњМРЧ ЛѓХТЗЮ СјЧрЧбДй (И№Еч ЙнРРРК ЙЋСњМАЁ СѕАЁЧЯДТ ЙцЧтРИЗЮ СјЧрЕШДй). БзЗГПЁЕЕ КвБИЧЯАэ АэЕЕРЧ СњМИІ АЁСј Л§ЙААшАЁ ППЊЧаРћРИЗЮ АЁДЩЧб РЬРЏДТ Бз СжКЏРЧ ПЃЦЎЗЮЧЧ СѕАЁПЁ РЧЧи АЁДЩЧЯДй (Ся, КИДй ИЙРК ЙЋСњМИІ ЙйХСРИЗЮ КИДй РћРК ОчРЧ СњМИІ БИУр). ЕћЖѓМ ЙЋСњМДТ АшПЭ СжРЇРЧ ЧеРИЗЮ ЦЧДмЕШДй.
АшПЭ СжРЇРЧ ПЃЦЎЗЮЧЧ ЧеРЬ ПЕКИДй ХЉИщ Бз АњСЄРК РкЙпРћРИЗЮ РЯОюГЏ Мі РжДй. (ПЃЦЎЗЮЧЧ: АшРЧ ЙЋСњМРЧ УДЕЕ)
ЁтSuniv = ЁтSsys + ЁтSsur > 0
ПЃЦЎЗЮЧЧРЧ СЄРЧ: S = klnW (k, Boltzman constant; W, ГЛКЮПЁГЪСіРЧ КЏШОјРЬ АшИІ ЙшПНУХГ Мі РжДТ ЙцЙ§РЧ Мі)РЬДй. ЕћЖѓМ ОюЖВ ШЧеЙАРЧ Р§ДыРћРЮ ПЃЦЎЗЮЧЧДТ translational, vibrational, rotational parameterЕщРЬ ОЫЗССЎ РжДйИщ ХыАшПЊЧаРћРЮ ЙцЙ§РИЗЮ АшЛъЕЩ Мі РжРИГЊ, КёБГРћ РлРК КаРкРЧ АцПьПЁИИ СїСЂРћРЮ АшЛъРЬ АЁДЩЧЯАэ КаРкАЁ ФПСіИщ АшЛъРК КвАЁДЩ ЧиСјДй.
РЬПЁ ЕћЖѓ ЛѕЗЮПю ЧдМіРЮ РкРЏПЁГЪСі АГГфРЬ Josiah W. GibbsПЁ РЧЧи ЕЕРдЕЧОњДй (1878Гт).
ЁтG = ЁтH-TЁтS
ЛѓПТРЧ ЦђЧќЛѓХТПЁМ ОюЖВ ЙнРРРЧ ПЃЦЎЗЮЧЧ КЏШДТ ЙнРРПРЧ КЏШИІ Р§ДыПТЕЕЗЮ ГЊДЋ АЊАњ ААДй. ЁтS = ЁтH/TПЁМ ЁтH-TЁтS = 0 ЕћЖѓМ ЛѕЗЮПю ЧдМі GИІ ЕЕРдЧЯПЉ, ЁтG = ЁтH-TЁтS ЁтH Ёж ЁтE РЬЙЧЗЮ ОюЖВ ЙнРРРЧ ЁтGДТ ГЛКЮ ПЁГЪСіПЭ АшРЧ ПЃЦЎЗЮЧЧ КЏШПЁ ЕћИЅДй. АЁЗЩ ATPРЧ АЁМіКаЧи АцПь ЧЅСиСЖАЧПЁМ РкРЏПЁГЪСі АЊРЧ КЏШДТ -7.7kcal/mol РЮЕЅ ЁтHИІ УјСЄЧЯИщ -4 kcal/molРЬ ОђОюСјДй. РЬЖЇ ГЊИгСі 3.7 kcal/molРК Л§МКЙАПЁ СѕАЁЕШ ЙЋСњМРЧ ЧќХТЗЮ СИРчЧЯДТ АЭРЬДй. |
ЁтG = 0 (ЦђЧќ) ПЁГЪСі ЙцУтРЬ ОјРН
ЁтGЁД 0 (ПЁГЪСі ЙцУтЙнРР: exergonic)
ЁтG ЁЕ0 (ПЁГЪСі ШэМіЙнРР: endergonic)
A. ЁтGЗЮМ ЙнРРРЧ РкЙпМКРЛ АсСЄЧв Мі РжДй. РЬЖЇ Р§ДыАЊРЧ УјСЄРК КвАЁДЩЧЯАэ, КЏШАЊРЮ ЁтG ЗЮ УјСЄЕШДй.
B. ЙнРРАцЗЮПЭДТ ЙЋАќЧЯДй (АЁЛъРћРЬДй). РкРЏПЁГЪСіРЧ КЏШДТ пШПТ, пШОаПЁМ РЯОюГЊДТ ЙнРРПЁМ РЬЗаРћРИЗЮ ОђОюСњ Мі РжДТ УжДыЧбРЧ РЏПыЧб РЯПЁ ДыЧб СЄЗЎРћ УјСЄАЊРЬДй. БзЗЏГЊ НЧСІЗЮ ОђОюСіДТ РЯРЧ ОчРК АцЗЮПЁ ДоЗСРжБт ЖЇЙЎПЁ ОЦЙЋИЎ РкРЏПЁГЪСі АЊРЬ ГЗРК РНРЧ АЊРЛ АЁСјДй ЧЯДѕЖѓЕЕ РќЧє ОђОюСіСі ОЪРЛ МіЕЕ РжДй (АЁЗЩ БлЗчФкПРСюАЁ УМГЛПЁМ ЛъШАњСЄРЛ ЙтРЛ ЖЇ ОђОюСіДТ ПЁГЪСіРЧ ОчРК НЧСІ РкРЏПЁГЪСі КЏШАЊРЧ 1/3 СЄЕЕ).
C. ЙнРРМгЕЕПЭДТ ЙЋАќЧЯДй.
1-2. Л§ЙАУМПЁМ ППЊЧаРЧ СпПфМК
ППЊЧаРК Л§ЙАУМПЁ РжОю СзДРГФ ЛчДРГФИІ АсСЄЧЯДТ СпПфЧб ЙЎСІРЬДй: Л§ШЧаПЁ РжОю ППЊЧаРЧ РЏПыМКРК ЙЋОљКИДйЕЕ ЦЏСЄЧб ШЧаЙнРРРЬ РкЙпРћРИЗЮ РЯОюГЏ АЭРЮСіИІ ПЙУјЧЯДТ АЭРЬДй. АЃДмЧб ПЙЗЮ ОюЖВ ШЧеЙАРЬ Л§ЙАУМПЁАд ПЁГЪСіПјРИЗЮ РЬПыЕЩ Мі РжАкДТАЁ ЧЯДТ АЭРЬДй. ПьИЎДТ АцЧшРИЗЮ РЏБтЙАРЬ КаРкЛъМвПЁ РЧЧи ЛъШЕЧИщ ПЁГЪСіИІ ЙцУтЧбДйДТ АЭРЛ ОЫАэ РжДй. ПЙИІ ЕщОю ГЊЙЋГЊ МЎХКРК ХИИщМ ИЙРК ПРЛ ГНДй. КёНСЧЯАд Л§ЙАУМЕщРК ХКМіШЙАРЬГЊ СіЙц, ДмЙщСњ ЕюРЛ ЛъШНУХАИщМ ПЁГЪСіИІ ОђДТДй. ОюЖВ Л§ЙАУМЕщРК hydrocarbonЕщРЛ ЛъШЧЯАэ, ОюЖВ АЭЕщРК ШЏПјЕШ sulfur ГЊ ironРЛ ЛъШНУХАБтЕЕ ЧбДй. БзЗЏГЊ ОюЖВ Л§ЙАУМЕЕ КаРкСњМвИІ ЛъШНУФб ЛьОЦАЅ МіДТ ОјДй. Бз РЬРЏДТ ЙЋОљРЮАЁ ? Бз ЧиДфРЬ ЙйЗЮ ППЊЧаПЁ РжДй. Бз ЙнРРРК РкЙпРћРИЗЮ РЯОюГЏ Мі ОјДТ АЭРЬДй. РЬЗЏЧб ПЙДТ И№Еч Л§ИэРЧ СЖР§ПЁ РжОю ППЊЧаРЧ СпПфМКРЛ КИПЉСжДТ АЭРЬДй. И№Еч Л§ЙАУМЕщРК БзЕщРЧ СжКЏРИЗЮКЮХЭ ШЧаПЁГЪСіИІ ОђРИИч ЛьОЦАЁБт ЖЇЙЎПЁ ППЊЧаРК КёЙаНКЗЏПю ДыЛѓРЬ ОЦДЯЖѓ СзДРГФ ЛчДРГФЧЯДТ НЩАЂЧб ДыЛѓРЮ АЭРЬДй.
ППЊЧаРК ЙнРРРЧ РкЙпМКРЛ АсСЄЧбДй: ПьИЎДТ ППЊЧаРЬ ОюЖВ ЙнРРРЬ "РЯОюГЏ Мі РжДТСі"ИІ АсСЄЧбДйАэ ИЛЧбДй. ПжГФЧЯИщ ППЊЧаРК Бз ЙнРРРЬ ЧбСЄЕШ НУАЃ ГЛПЁ РЯОюГДйАЁ ОЦДЯЖѓ Бз ЙнРРРЬ АЁДЩЧбСі ПЉКЮИІ КИПЉСжБт ЖЇЙЎРЬДй. ППЊЧаРћРИЗЮ АЁДЩЧб ЙнРРРЬ РЯОюГЊДТ МгЕЕДТ Бз ЙнРРРЧ ММКЮРћРЮ БтРлПЁ ДоЗСРжДй. ОюЖВ Л§ШЧаРћ ЙнРРРЬ НХМгШї РЯОюГЊЗСИщ РћР§Чб ШПМвАЁ ЧЪПфЧб АЭРЬДй. РЬПЭ ААРК ЙнРРРЧ РкЙпМКАњ МгЕЕПЭРЧ БИКаРК ШЧаРкКИДйДТ ЦЏШї Л§ШЧаРкПЁАд СпПфЧЯДй. ПжГФЧЯИщ ШЧаЙнРРРЧ АцПьДТ ОаЗТРЬГЊ ПТЕЕ, ЙнРРЙАРЧ ГѓЕЕ ЕюРЛ КЏШНУХГ Мі РжБт ЖЇЙЎРЬДй. ЙнИщПЁ Л§ИэУМДТ ШЮОР СІЧбЕШ ЛѓХТПЁ РжОюМ АХРЧ АэСЄЕШ ПТЕЕГЊ ОаЗТ, БзИЎАэ СІЧбЕШ ЙќРЇРЧ ЙнРРЙАПЁМИИ БтДЩРЛ Чв Мі РжДй.
1-3. ДмЙщСњРЧ СЂШћАњ ППЊЧа (БГАњМ 171 ЦфРЬСі ТќСЖ)
ДмЙщСњРК ЧЎИЎИщМ БиМКАњ КёБиМК ОЦЙЬГыЛъ АчЛчННЕщРЬ ПыОзПЁ ГыУтЕШДй.
1. ЧзЛѓ -TЁтSchain > 0 РЬДй. ПжГФЧЯИщ ЧЎИА ЛѓХТПЁМДТ СЂШљ ЛѓХТКИДй Дњ СЄЕЗЕЧОю РжРИЙЧЗЮ ЁтSchain РК РНМіАЊРЬБт ЖЇЙЎРЬДй.
2. ЧзЛѓ -TЁтSsolvent < 0 РЬДй. ПжГФЧЯИщ ЙАКаРкПЁ СњМИІ АПфЧЯБт ЖЇЙЎРЬДй.
КёБиМКАњ БиМК АчЛчННЗЮ БИКаЧЯПЉ КИИщ,
КёБиМК БтПЁМДТ ЁтG < 0
ЁтHchain = ЁтHf - ЁтHu > 0 : fold ЛѓХТПЁМРЧ ОрЧб ЙнЕЅИЃЙпНК ШћКИДй unfold ЛѓХТПЁМ ПыОзАњРЧ ЛѓШЃРлПыРЬ Дѕ ХЉДй. ПжГФЧЯИщ ЦюУФСј ЛѓХТПЁМДТ ЙААњРЧ ЛѓШЃРлПыРЬ ХЉБт ЖЇЙЎРЬДй.
ЁтHsol = ЁтHf - ЁтHu < 0 : СЂЧєСќРИЗЮНс ЙАКаРкАЃРЧ ЛѓШЃРлПыРЬ СѕАЁЧЯБт ЖЇЙЎ. БзЗИСіИИ МЗЮ ЛѓМтЕЧБт ЖЇЙЎПЁ РќУМРћРЮ ЁтHРЧ ШПАњДТ РлДй.
ЁтSsolvent > 0 : КёБиМК БтЕщРК ЦюУФСј ЛѓХТПЁМ ЙАКаРкЕщПЁ СњМИІ АПфЧЯБт ЖЇЙЎРЬДй.
БиМКБтПЁМ ЁтG ДТ АХРЧ 0ПЁ АЁБѕДй.
ЁтHchain > 0
ЁтHsol < 0
ЁтSsolvent > 0 : БиМККаРк СжКЏПЁМЕЕ ЙАКаРкЕщРК ОюДР СЄЕЕ СњМИІ АПфЙоДТДй.
ЕћЖѓМ ДмЙщСњ БИСЖРЧ ОШСЄМКПЁ АЁРх ХЋ ПЕЧтРЛ ЙЬФЁДТ ПфМвДТ ЙйЗЮ КёБиМКБтПЁ ДыЧб ЁтSchain ЖѓДТ АЭРЬ ИэШЎЧЯДй.
2. ЧЅСиЛѓХТПЭ ЧЅСиРкРЏПЁГЪСі КЏШ
ЧЅСиЛѓХТ (ЧЅСиСЖАЧ ЧЯПЁМРЧ ЛѓХТ): Л§ИЎРћРЮ СЖАЧРК И№ЕЮ ДйИЃБт ЖЇЙЎПЁ ЛѓДыРћРЮ КёБГИІ РЇЧи ЧЅСиСЖАЧРЛ МГСЄ
pure solids, pure liquids, 1 БтОаРЧ gas
АЂ МККаРЧ УЪБтГѓЕЕАЁ 1 M, pH 7.0, ЛѓПТ (25ЁЩ)
ШЧаАњ ЙАИЎЧаПЁМ ЛчПыЧЯДТ ЧЅСиЛѓХТПЭ Л§ШЧаПЁМ ЛчПыЧЯДТ ЧЅСиЛѓХТПЭРЧ ТїРЬАЁ РжДй.
Л§ЙАУМДТ pH 7.0Ањ ЛѓПТ ЛѓХТПЁ РжРИИч, ЙАПЁ СИРчЧбДй.
ЕћЖѓМ KeqПЭ Keq'ПЁДТ ТїРЬАЁ РжДй. Keq'ПЁДТ [H+]ПЭ [H2O]АЁ ЦїЧдЕЧОю РжДй.
A + B ЙнРРРЬ ЦђЧќПЁ ЕЕДоЧЯИщ aA + bB Ёъ cC + dD
ЁтG = ЁтGo' + RT 
ЁтGo : ЧЅСиРкРЏПЁГЪСі КЏШ, ЙнРРЙАРЧ КЛСњ
ЁтGo' : pH 7ПЁМРЧ ЧЅСиРкРЏПЁГЪСі КЏШ
R: gas constant, 8.31 J/mol K
RT : ЙнРРЙАРЧ ГѓЕЕ
: ЙнРРЙАРЧ ГѓЕЕ
ЦђЧќЛѓХТПЁМ ЁтG = 0 РЬЙЧЗЮ
0 = ЁтGo' + RT 
1 M, 1 atm РЧ ЧЅСиЛѓХТПЁМ
ЦђЧќЛѓМі
ЁтGo' = - RT 
=
-2.303 RT  = -2.303 x 1.98 x 10-3 x 298 x
= -2.303 x 1.98 x 10-3 x 298 x 
ЦђЧќЛѓХТПЁМ ЙнРРЙААњ Л§МКЙАРЧ ГѓЕЕИІ ОЫИщ ЦђЧќЛѓМі Keq'РЧ АшЛъРЬ АЁДЩЧЯАэ ЕћЖѓМ ЁтGo'РЧ АшЛъЕЕ АЁДЩЧиСјДй.
Keq' = 10-ЁтGo'/2.303RT = 10-ЁтGo/1.36
Keq' |
ЁтGo' |
10-4 |
5.46 |
10-1 |
1.36 |
1 |
0 |
10 |
-1.36 |
Keq' = 0.0475 РЬАэ, AРЧ УЪБтГѓЕЕДТ 2 X 10-4 M, BРЧ УЪБтГѓЕЕДТ 3 X 10-6 M РЮ A Ёц B ЙнРРРЧ ЁтG ДТ ?
ЁтGo' = -2.303 RT 
=
-2.303 RT 
= 1.8 kcal/mol
ЁтG = 1.8 + 2.303 RT 
= 1.8 - 2.5
= - 0.7 kcal/mol
*ЙнРРПЁ РжОюМ РкЙпМКРЧ БтСиРК ЁтGo' АЁ ОЦДЯЖѓ ЁтG РЬДй.
ШЧаРћРИЗЮ ТІСіПіСј РЯЗУРЧ ЙнРРЕщПЁ ДыЧб РќУМ РкРЏПЁГЪСі КЏШДТ АГАГРЧ ДмАшЕщРЧ РкРЏПЁГЪСі КЏШРЧ ЧеАњ ААДй.
ЕћЖѓМ ЧЅСиСЖАЧЧЯПЁМ РќУМРЧ ЧеРЬ РНРЧ АЊРЛ АЁСіИщ ПЌАсЕШ ЙнРРЕщРК РкЙпРћРИЗЮ СјЧрЕЩ Мі РжДй.
A Ёц B + C ЁтGo'= +5 kcal/mol
BЁц D ЁтGo'= -8 kcal/mol
----------------------------------------------
A Ёц C + D ЁтGo'= -3 kcal/mol
ППЊЧаРћРИЗЮ КвИЎЧб ЙнРРРЬ БзАЭАњ ПЌАсЕШ ППЊЧаРћРИЗЮ ССРК ЙнРРПЁ РЧЧи УпСјЕЩ Мі РжДй (АјХыРћРЮ СпАЃЛъЙАРЮ BПЁ РЧЧи ПЌАсЕЧОю РжДй). РЬАЭРЛ ПЁГЪСі ПЌАс (energy coupling)РЬЖѓ ЧбДй. Л§УМ ГЛПЁМ РЬЗЏЧб ПЁГЪСі ПЌАсПЁДТ ММАЁСі ЧќХТАЁ РЬПыЕШДй.
by ATP: РкРЏПЁГЪСіРЧ РќДоРк
by conformational changes
by the flow of ions across membranes
РЬСпПЁМЕЕ ATPДТ Л§УМАшПЁМ РЯОюГЊДТ ПЁГЪСі БГШЏПЁ РжОюМ СпУпРћРЮ ПЊЧвРЛ ЧбДй.
ППЊЧаРћРИЗЮ КвИЎЧб ШЧаЙнРРРЧ СјЧрРК ДйРН ЕЮАЁСі ЙцЙ§ПЁ РЧЧи РЬЗчОюСјДй.
(1) driven by the subsequent reaction
k1 k2
A Ёц B Ёц C
k1 = 0.1 = [B]/[A]
k2 = 100 = [C]/[B]
РќУМ ЙнРР k1 k2 = [B]/[A] x [C]/[B]
= [C]/[A] = 0.1 x 100 = 10
(2) driven by ATP
ATP АЁМіКаЧиДТ ПЌАсЕШ ЙнРРЕщРЧ ЦђЧќРЛ 108 РЧ АіРИЗЮ СѕАЁНУХВДй.
ДйРНАњ ААРК АњСЄРЛ АЁСЄЧиКИРк.
A Ёц B : ЁтGo'= + 4 kcal/mol
25 ЁЩПЁМ Keq' = [B]eq /[A]eq
= 10 -ЁтGo'/1.36 = 1.15 x 10-3
AПЁ ДыЧб BРЧ ИєКёАЁ 1.15 x 10-3 Ањ АААХГЊ Дѕ ХЌ ЖЇ AДТ РкЙпРћРИЗЮ BЗЮ РќШЏЕЩ Мі ОјДй. БзЗЏГЊ [B]/[A] > 1.15 x 10-3 РЯ ЖЇ ATPПЭ ТІСіПіСіИщ
A + ATP + H2O Ёц B + ADP + pi + H+
ЁтGo' = -7.3 + 4 = -3.3 Kcal/mol
Keq' =
([B]eq/[A]eq) x ([ADP]eq [pi]eq/[ATP]eq) =  = 2.67 x 102
= 2.67 x 102
ММЦї ГЛРЧ [ATP]/([ADP][pi])РЧ КёДТ 500 РЬЙЧЗЮ

Ся, 1.34 x 105/ 1.15 x 10-3 = 108
2. ATP : ПЁГЪСі РќДоРк
ATPДТ adenine, ribose, triphosphate unitЗЮ БИМКЕЧИч КИХы Mg++ , Mn++ПЭРЧ complexЗЮ СИРч
ATPДТ energy rich molecule: ЛяРЮЛъБтАЁ ЕЮАГРЧ ЙЋМі РЮЛъАсЧеРЛ РЬЗчАэ РжБт ЖЇЙЎПЁ АэПЁГЪСі КаРкЗЮ РлПыЧбДй. РЬ ЙЋМіРЮЛъ АсЧеРЬ АЁМіКаЧиЕЧИщМ АЂАЂ - 7.3 kcal/mol РЧ ЁтGo'ИІ ЙцУтЧбДй. НЧСІЗЮДТ ДмМјЧб АЁМіКаЧиПЁ РЧЧб ПЁГЪСі ЙцУтРЬ ОЦДЯЖѓ БзЗь РќРЬПЁ РЧЧб ПЁГЪСі АјБоРЬДй. ЕћЖѓМ АэПЁГЪСі РЮЛъШЧеЙА ЖЧДТ АэРЮЛъБт РќДо РќРЇИІ АЁСјДйАэ ИЛЧЯДТ АЭРЬ СЄШЎЧЯДй. ДйИИ БйРАМіУрПЁМ ATPРЧ РлПыРК ДмМјШї АЁМіКаЧиПЁ РЧЧб АЭРЬДй.
ATP + H2O Ёц ADP + pi + H+
ATP + H2O Ёц AMP + ppi + H+
РЬЕщ ATP, ADP, AMP ЕщРК adenylate kinaseПЁ РЧЧи ЛѓШЃРќШЏРЬ РЬЗчОюСјДй. РЬ ШПМвДТ ATP + AMP Ёц 2 ADP ЙнРРРЛ УЫИХЧбДй. АЁМіКаЧиПЁ ЕћИЅ ЁтGo'АЊРК РЬПТГѓЕЕПЭ Mg++, Ca++РЧ ГѓЕЕПЁ ЕћЖѓ ОрАЃОП ДйИЃДй.
2-1. ATPАЁ РкРЏПЁГЪСіРЧ ИХАГУМ ПЊЧвРЛ ЧЯДТ РЬРЏ
(1) interconvertable (ATP-ADP cycle); РќЧќРћРЮ ММЦїПЁМ ATP КаРкДТ Л§МКЕШСі 1Ка РЬГЛПЁ МвКёЕШДй. Ся, ATPДТ ИХПь НХМгЧЯАд РќШЏРЬ РЬЗчОюСјДй. ATPДТ РкРЏПЁГЪСіРЧ long-term storageАЁ ОЦДЯЖѓ immediate donorЗЮ ЛчПыЕШДй (ЧЯЗч 2500 kcalРЧ ПЁГЪСіИІ МвИ№ЧбДйАэ АЁСЄЧЯИщ 2500/7.3 = 350 molРЧ ATP Л§МКРЬ ЧЪПфЧЯДй. БзЗЏГЊ НЧСІ Л§УМ ГЛ СИРчЧЯДТ ОчРК 0.1 molПЁ СіГЊСі ОЪДТДй).
(2) intermediate group-transfer potential
(3) ATP has high energy bonds; ATPДТ БИСЖРћРИЗЮ ГєРК РЮЛъБт РќДо РќРЇИІ АЁСјДй. ММАЁСіРЧ РЬРЏАЁ РжДй.
УЙТА, electrostatic repulsion(СЄРќБтРћ ЙнЙп)РЬ ADPПЁМ ШЮОР ОрЧЯДй.(pHПЭ Mg++ ГѓЕЕПЭЕЕ АќЗУ)
ЕбТА, ПыЧиЕЕДТ ADPПЭ piАЁ ШЮОР ССДй: pHАЁ СѕАЁЧЯИщМ РНРќЧЯАЁ СѕАЁЧЯПЉ ATPРЧ СЄРќБтРћ БфРхРК СѕАЁЧбДй.
ММТА, resonance stabilization(АјИэОШСЄШ); ADPПЭ PiДТ ATPКИДй ШЮОР ССРК АјИэОШСЄШИІ ДЉИАДй.